近日,广州医科大学附属第二医院微创介入科朱康顺教授团队在国际肝病学顶级期刊Journal of Hepatology发表重磅研究,首次揭示TACE术后肠道菌群紊乱是导致肝损伤的关键新机制,并发现补充益生菌罗伊氏乳杆菌或其代谢产物吲哚-3-乳酸(ILA)可有效缓解肝损伤,为肝癌介入术后肝保护提供了全新策略。

据了解,TACE术后,患者常出现肝功能损伤,少数严重者甚至进展为肝衰竭。传统观点认为,这种损伤主要源于栓塞导致的肝脏缺血或化疗药物的直接毒性。然而,临床上患者TACE术后肝损伤程度差异较大,其深层机制一直未明。
“我们在临床工作中发现,有的患者栓塞量不大,却出现肝功能明显下降;有的栓塞范围很大,肝功能受损程度反而相对有限。这促使我们思考,除了手术操作本身,是否还有其他机制在起作用?”广医二院微创介入科主任朱康顺教授在接受采访时回忆道。
正是基于这样的临床困惑,朱康顺教授团队将目光投向了“肠-肝轴”。肠道与肝脏通过门静脉紧密相连,形成复杂的“肠-肝循环”。近年来,肠道菌群紊乱在多种肝病进展中的作用日益受到重视。
该团队开展了一项历时数年的研究,创新性地从肠道微生态视角切入,最终在国际上首次揭示:TACE术后肠道稳态失衡、特定益生菌减少,是加重术后肝损伤的重要新机制。
研究发现,TACE术后,患者肠道内一种名为罗伊氏乳杆菌(Limosilactobacillus reuteri)的益生菌及其关键代谢产物吲哚-3-乳酸(ILA)的丰度显著降低。而这种降低与患者术后肝损伤的严重程度及远期生存具有相关性。
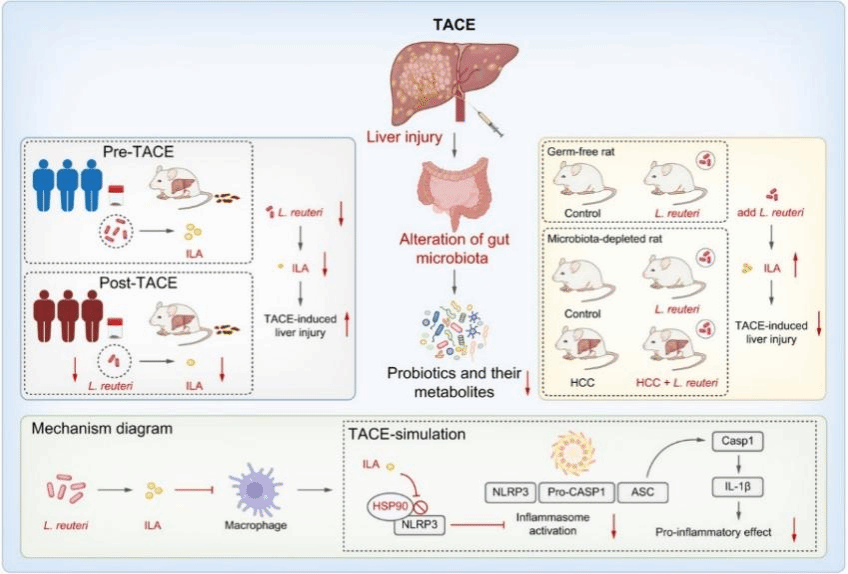
为验证因果关系,团队构建了大鼠TACE模型,并突破技术瓶颈,创新性地通过尾动脉路径实现大鼠肝动脉超选介入。“小动物的血管比人体要细得多,这即便对于我们已有多年介入手术经验的临床医生来说,也颇具挑战性。团队通过大鼠尾动脉路径实现肝动脉插管进行介入治疗,手术时间从最初90分钟,现在已优化至15~30分钟。”共同通讯作者林立腾副教授介绍。实验发现,补充罗伊氏乳杆菌或ILA可显著改善大鼠TACE术后肝损伤。
进一步机制研究表明,ILA能直接结合热休克蛋白90(HSP90),抑制肝脏巨噬细胞中NLRP3炎症小体的过度激活,从而减轻肝脏内过度的炎症反应,保护肝脏实质细胞。
全球知名肝病及肠道微生态学专家、美国加州大学圣地亚哥分校Bernd Schnabl教授发表述评并高度评价该研究:“这项研究通过肠道菌群代谢的视角,回答了目前肝癌TACE介入治疗所面临的重大临床问题,提出了通过外源性添加益生菌或其代谢物来维护肠道稳态、保护肝功能的全新策略,为‘microbiome-informed hepatology(微生物组整合肝脏病学)’提供了全新的范式。”
需要特别提醒的是,尽管研究显示菌群调控潜力巨大,团队强调,目前暂不推荐患者自行补充益生菌来防治TACE介入治疗后肝功能受损的问题。“个体差异大,仍需通过大样本、多中心、前瞻性临床试验确定菌种、剂量和适用人群。”朱康顺教授表示,团队已启动多中心临床研究,推动个体化菌群干预方案落地。
与此同时,团队在肝癌联合治疗领域另一突破性成果同期发表:全球首次报道钇-90微球内放射治疗(SIRT)联合靶向及免疫疗法(SIRT-L-P)对高肿瘤负荷肝癌的疗效优于传统TACE方案。研究显示,SIRT-L-P组中位无进展生存期达12.1个月,显著优于TACE-L-P组的9.0个月,且不良反应更低。
“科研是学科发展的灵魂。只有解决临床真问题,才能持续提升疗效。”朱康顺教授指出,团队坚持临床与科研结合,从大量个案中提炼规律。例如,通过分析长期生存患者特征,发现肠道菌群稳态与预后密切相关,进而反哺治疗策略优化。
未来,团队计划开展SIRT-L-P方案的前瞻性研究,并深化菌群调控的转化应用。正如朱康顺教授所言:“从肠道健康切入肝病治疗,只是起点。我们目标是推动肝癌治疗迈向微生态精准干预的新阶段。”